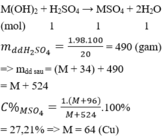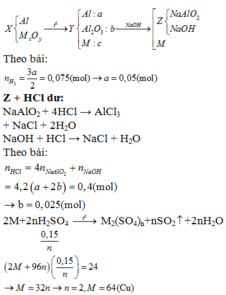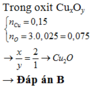Hòa tan hết một lượng kim loại M trong dung dịch H2SO4 20% (loãng, dư 20% so với lượng cần phản ứng), thu được dung dịch chứa muối trung hòa có nồng độ là 23,68% và axit dư. Tìm M.

Những câu hỏi liên quan
hòa tan hoàn toàn một lượng kim loại M trong dd H2SO4 loãng có nồng độ 20% (lấy dư 20% so với lượng cần cho pứ). Dung dịch hu đc có nồng độ của muối tạo thành là 23,68%. Xác định kim loại M?
Gọi M hóa trị n
Giả sử có 1 mol H2SO4 pư
---> Khối lượng dd H2SO4 đã pư = 1*98*100/20 = 490g
---> khối lượng lấy : mdd = 490 + 490*0.2 = 588 g
2M + nH2SO4 ---> M2(SO4)n + nH2
2/n<----1-------------->1/n ------>1
Khối lượng dd sau khi pư = 588 + 2M/n -2*1 = 586 + 2M/n
Khối lượng muối = 1/n*(2M + 96n)
Vậy ta có pt: [1/n*(2M + 96n)]/ [586 + 2M/n] = 0.2368 ---> M/n = 28
--> M = Fe, n = 2
Đúng 0
Bình luận (0)
Giả sử có 1 mol H2SO4 pư
---> Khối lượng dd H2SO4 đã pư = 1*98*100/20 = 490g
---> khối lượng lấy : mdd = 490 + 490*0.2 = 588 g
2M + nH2SO4 ---> M2(SO4)n + nH2
2/n<----1-------------->1/n ------>1
Khối lượng dd sau khi pư = 588 + 2M/n -2*1 = 586 + 2M/n
Khối lượng muối = 1/n*(2M + 96n)
Vậy ta có pt: [1/n*(2M + 96n)]/ [586 + 2M/n] = 0.2368 ---> M/n = 28
--> M = Fe, n = 2
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 1 lượng kim loại M trong dung dịch H2SO4 loãng có nồng độ 20% (lấy dư 20% so với lượng cần cho phản ứng). Dung dịch thu được có nồng độ của muối tạo thành là 23.68%. Xác định kim loại M?
Giả sử ban đầu có 1,2 mol H2SO4\(\rightarrow\)mdd=588g\(\rightarrow\)nH2SO4 phản ứng=1mol\(2M+nH_2SO_4\rightarrow M_2\left(SO_4\right)_n+nH_2\)Dễ thấy \(nH_2=nSO^{2-}_4=1\) tạo muôi\(\frac{m+96}{m+588-2}=0,2368\rightarrow m=56\)\(\frac{56}{M}n=2.nSO^{2-}_4\)với n là hoá trị M M là Fe
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn một lượng kim loại M trong dung dịch H2SO4 loãng có nồng độ 20%(lấy dư 20% so với lượng cần cho phản ứng). Dung dịch thu được có nồng độ của muối tạo thành là 23,68%. Xác định kim loại M
-Chọn số mol H2SO4 ban đầu là 1 mol\(\rightarrow\)số mol H2SO4 phản ứng là 1.\(\dfrac{80}{100}=0,8mol\)
\(m_{dd_{H_2SO_4}}=\dfrac{1.98.100}{20}=490gam\)
2M+nH2SO4\(\rightarrow\)M2(SO4)n+nH2
\(\dfrac{1,6}{n}\)\(\leftarrow\)0,8\(\rightarrow\).....\(\dfrac{0,8}{n}\)........0,8
\(m_{dd}=\dfrac{1,6}{n}M+490-0,8.2=\dfrac{1,6}{n}M+488,4\)
C%M2(SO4)n=\(\dfrac{\dfrac{0,8}{n}.\left(2M+96n\right)}{\dfrac{1,6}{n}M+488,4}.100=23,68\)
\(\rightarrow\)\(\dfrac{160M}{n}+7680=\dfrac{37,888M}{n}+11565,312\)
\(\rightarrow\)\(\dfrac{122,112M}{n}=3885,312\)
M=32n
n=1\(\rightarrow\)M=32(loại)
n=2\(\rightarrow\)M=64(Cu)
n=3\(\rightarrow\)M=96(loại)
-Vậy M là Cu
Đúng 1
Bình luận (0)
Câu 2: Hòa tan hoàn toàn một lượng kim loại M trong dung dịch H2SO4 loãng có nồng độ 20% (lấy dư 20% so với lượng cần cho phản ứng). Dung dịch thu được có nồng độ của muối tạo thành là 23,68%. Tìm kim loại M?
Khi hòa tan hiđroxit kim loại
M
(
O
H
)
2
bằng một lượng vừa đủ dung dịch
H
2
S
O
4
20%, thu được dung dịch muối trung hòa có nồng độ 27,21%. Kim loại M là A. Cu B. Zn C. Fe D. Mg
Đọc tiếp
Khi hòa tan hiđroxit kim loại M ( O H ) 2 bằng một lượng vừa đủ dung dịch H 2 S O 4 20%, thu được dung dịch muối trung hòa có nồng độ 27,21%. Kim loại M là
A. Cu
B. Zn
C. Fe
D. Mg
Khi hòa tan hidroxit kim loại M(OH)2 bằng một lượng vừa đủ dung dịch H2SO4 20%, thu được dung dịch muối trung hòa có nồng độ 27,21%. Kim loại M là:
A. Cu
B. Zn
C. Fe
D. Mg
Đáp án A.
Coi nH2SO4 = 1 mol
M(OH)2 + H2SO4 → MSO4 + 2H2O
mdd H2SO4= 1.98.100/20 = 490 (gam)
=> mdd sau = (M + 34) + 490 = M + 524

Đúng 0
Bình luận (0)
Khi hòa tan hiđroxit kim loại M(OH)2 bằng một lượng vừa đủ dung dịch H2SO4 20% thu được dung dịch muối trung hòa có nồng độ 27,21%. Kim loại M là:
A. Fe
B. Zn
C. Cu
D. Mg
Đáp án C
Giả sử đem 1 mol H2SO4 phản ứng, ta có:
![]()
mdung dịch sau phản ứng = 490 + (M + 34) (gam)
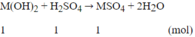
Theo đề bài ta có:
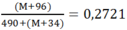
⇒ M = 64: Đồng
Đúng 0
Bình luận (0)
Hòa tan M gam kim loại R ( có một hóa trị duy nhất ) vào dung dịch H2SO4 loãng dư sau phản ứng thấy khối lượng dung dịch tăng 1,2 gam so với dung dịch axit ban đầu nung lượng kim loại R nói trên ngoài không khí đến khối lượng không đổi thu được 2,55 gam chất rắn . Thấy có V lít không khí ( đktc ) tham gia phản ứng.
a ) Xác định kim loại R và tính m
b ) tính V ( biết oxi chiếm khoảng 20% thể tích không khí )
Đọc tiếp
Hòa tan M gam kim loại R ( có một hóa trị duy nhất ) vào dung dịch H2SO4 loãng dư sau phản ứng thấy khối lượng dung dịch tăng 1,2 gam so với dung dịch axit ban đầu nung lượng kim loại R nói trên ngoài không khí đến khối lượng không đổi thu được 2,55 gam chất rắn . Thấy có V lít không khí ( đktc ) tham gia phản ứng. a ) Xác định kim loại R và tính m b ) tính V ( biết oxi chiếm khoảng 20% thể tích không khí )
a)
Gọi số mol R là a (mol)
PTHH: 2R + nH2SO4 --> R2(SO4)n + nH2
a------------------------->0,5an
mtăng = mR - mH2 = a.MR - 2.0,5an = a.MR - an = 1,2 (1)
PTHH: 4R + nO2 --to--> 2R2On
a--------------->0,5a
=> \(0,5a\left(2.M_R+16n\right)=2,55\)
=> a.MR + 8an = 2,55 (2)
(1)(2) => a.MR = 1,35; an = 0,15
=> \(M_R=9n\left(g/mol\right)\)
Xét n = 3 thỏa mãn => MR = 27 (g/mol)
=> R là Al
a = 0,05 (mol)
m = 1,35 (g)
b)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,05->0,0375
=> VO2 = 0,0375.22,4 = 0,84 (l)
=> Vkk = 0,84 : 20% = 4,2 (l)
Đúng 2
Bình luận (2)
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm Al và một oxit kim loại trong khí trơ, thu được hỗn hợp Y. Cho Y vào dung dịch NaOH (loãng, dùng dư 20% so với lượng cần phản ứng), thu được dung dịch Z, chất không tan T và 1,68 lít khí
H
2
(đktc). Cho dung dịch HCl dư vào Z, thấy có 0,42 mol HCl phản ứng. Hòa tan hết T vào dung dịch
H
2
S
O
4
, thu được 24 gam muối sunfat...
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm Al và một oxit kim loại trong khí trơ, thu được hỗn hợp Y. Cho Y vào dung dịch NaOH (loãng, dùng dư 20% so với lượng cần phản ứng), thu được dung dịch Z, chất không tan T và 1,68 lít khí H 2 (đktc). Cho dung dịch HCl dư vào Z, thấy có 0,42 mol HCl phản ứng. Hòa tan hết T vào dung dịch H 2 S O 4 , thu được 24 gam muối sunfat và 3,36 lít khí S O 2 (ở đktc, là sản phẩm khử duy nhất của H 2 S O 4 ). Biết các phản ứng xảy ra hoàn toàn. Tổng số các nguyên tử trong công thức oxit kim loại ban đầu là
A. 2
B. 3
C. 5
D. 7